手ごわい血液の病気 特徴を知ろう『骨髄異形成症候群』
年のせいか、めまいがする、体がだるい、健康診断の血液検査で異常を指摘された……。もしかしたら、それは血液の病気かもしれません。高齢者に多く、白血病に進行することもある難治性の骨髄異形成症候群が疑われます。診断されたら、検査データに基づいてリスクを正しく予測し、それに応じた治療を受けることがポイントになります。今後、患者数の増加が懸念されるこの疾患についての基礎知識を紹介します。

近畿大学医学部 血液・膠原病内科 主任教授
松村 到 先生 (まつむら・いたる)
1984 年、大阪大学医学部卒業。市立伊丹病院内科医員、大阪大学医学部第二内科学教室、同バイオメディカル教育センター腫瘍病理学研究生、同血液・腫瘍内科助教授などを経て2011年より現職。2018 年より近畿大学医学部長、2022 年4 月より近畿大学副学長。日本血液学会理事長・血液指導医、日本内科学会評議員・内科指導医、日本臨床腫瘍学会協議員・指導医。JALSG(特定非営利活動法人 成人白血病治療共同研究機構)常務理事。
血球の減少と形態異常 急性骨髄性白血病にも
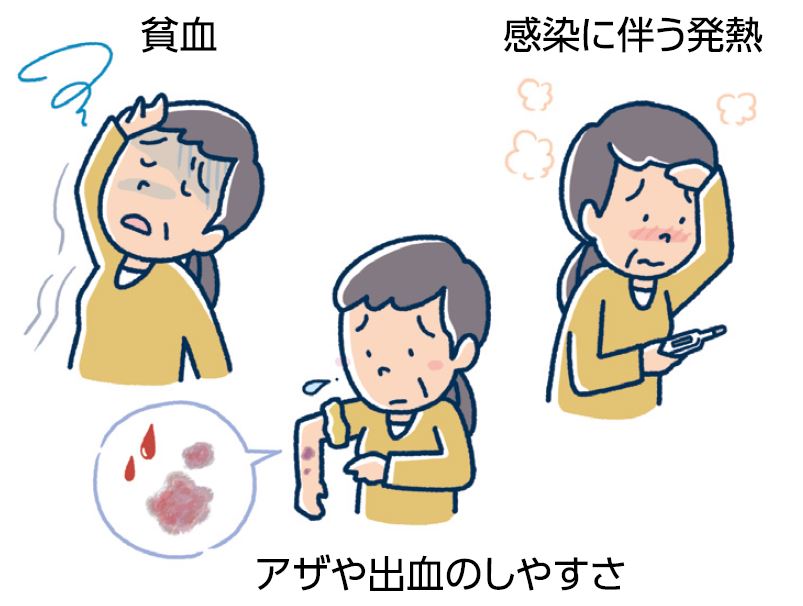
65歳のAさんは体力自慢だったのに、最近は疲れやすく、めまいや動悸、息切れがするのも気になります。
72歳のBさんはこのごろよく風邪をひきます。発熱がしつこく続き、風邪薬をのんでも治まりません。
58歳のCさんは、どこにもぶつけていないのにアザ(内出血)ができやすく、鼻血や歯茎からの出血もしばしばです。
いずれも血液のがんの1つ、骨髄異形成症候群において見られる症状です。血液を構成する血液細胞(赤血球、白血球、血小板)は、背骨や胸骨などの中心にある骨髄に存在する造血幹細胞からつくられます。その造血幹細胞に異常が生じ、形態異常の血液細胞がつくられたり(血球異形成)、正常な血液細胞が減ったり(血球減少)するために、さまざまな症状が起こります。
赤血球の異常は動悸などの貧血症状、白血球の異常は感染症や発熱、血小板の異常は出血のしやすさにつながります。自覚症状がなく、健康診断の血液検査で指摘されることも少なくありません。
さらに、より悪性度の高い急性骨髄性白血病へと移行するリスクがある(確率は10~20%)ことも、この病気の重大な特徴です。患者さんの骨髄や末梢血(血管を流れる血液)には芽球と呼ばれる未熟な血液細胞が存在しています。この芽球の割合が高いほど病状は進んでおり、20%を超えると急性骨髄性白血病と診断されます。
骨髄異形成症候群は中高年に多く、特に70歳以上で急激に増えますが、若くして発症することもあります。国内では1年間に約6000人が新たに診断され、男女比はおよそ2対1で男性のほうが多くなっています。
この病気は造血幹細胞の染色体・遺伝子変異によって起こりますが、多くの場合、染色体・遺伝子変異の発症メカニズムは不明です。
最新の研究で、血液検査は「正常」でまったく健康なのに、遺伝子レベルでは骨髄異形成症候群にかかわる変異を持つ人が、かなり多くいることが明らかになりました(70代で約10%)。
このような状態をCHIP(チップ)と呼び、CHIPに何らかの環境要因が重なり、さらに遺伝子異常が加わると、骨髄異形成症候群の発症につながることもわかっています。
血液と骨髄を精密検査 大事なのは予後の予測
骨髄異形成症候群は、過去の抗がん剤治療や放射線治療の影響で数年後に発症する(2次性骨髄異形成)こともあり、この病気全体の1~2割を占めます。高齢化社会が進み、さらにがん治療の進歩によりサバイバーと呼ばれる長期生存者が増えるにつれ、今後このようなほかの原因に基づく2次性の骨髄異形成症候群が増えることは避けられないでしょう。
診断に必須なのは血液検査、骨髄検査、染色体検査です。血液検査では各血球の数や形態異常、芽球の有無などを調べます。異常が発見されたら骨髄検査を行います。腸骨から骨髄液を採取して細胞を染色し、芽球の比率などを観察します。また、骨髄液を用いた染色体検査は診断・リスク分類に必要です。これらのデータから確定診断を行い、さらに細かくいくつかの病型に分類します。
骨髄異形成症候群は再生不良性貧血などとの鑑別が難しく、また血球減少や形態異常は感染症、肝臓病、薬物、飲酒などほかの原因でも起こるため、慎重に判断します。初診はかかりつけ医でも、精密検査や診断、治療は血液専門医を受診しましょう。
遺伝子変異の検査としては、一度に多くの遺伝子情報を調べられる遺伝子パネル検査がありますが、骨髄異形成症候群を含む血液のがんにはまだ保険適用されていません。近い将来の実現が期待されています。
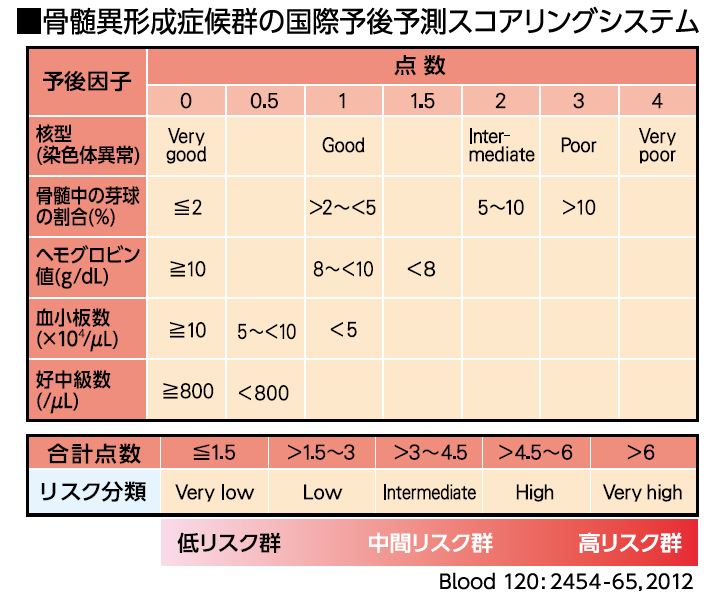
治療法を決めるにあたって行われるのが、予後(病状の見通し)の予測です。検査で得たデータ(骨髄中の芽球の割合、染色体異常、減少している血球の種類など)を点数化し、その合計点数により低リスク群、中間リスク群、高リスク群に分類します(下表)。この場合のリスクとは、急性骨髄性白血病へと進む可能性のことです。
低リスク判定なら輸血や 薬物療法で生活の質保つ
低リスクの場合、無症状ならば経過を観察します。貧血や感染症、出血など、血球減少に伴う症状があれば輸血が治療の柱となります。長期にわたって赤血球輸血を繰り返すと鉄分が内臓に蓄積し、心不全や肝不全、甲状腺機能低下、糖尿病などを招く鉄過剰症になるリスクがありますが、近年は鉄を排出する働きをする経口の鉄キレート剤が普及しており、安全に輸血を続けることができます。
輸血回数を抑えることは、生活の質の改善にもつながります。このため、赤血球産生を促すホルモンであるエリスロポエチンの濃度が低下している患者さんに対しては、ダルベポエチンなどのエリスロポエチン製剤(注射薬)が使われることもあります。一部の患者さんには免疫抑制剤が造血回復効果を発揮することがありますが、保険適用外です。
骨髄検査の結果、特別な染色体変異を持っていることがわかった人に対しては、レナリドミドを用います。赤血球を増やす高い効果があり、半数以上の患者さんが輸血に頼らずに済むようになったとの報告があります。ただ、投与の対象となる染色体変異を持つ患者さんはごく一部にとどまります。
高リスク者は移植を検討 さらに薬の選択肢も
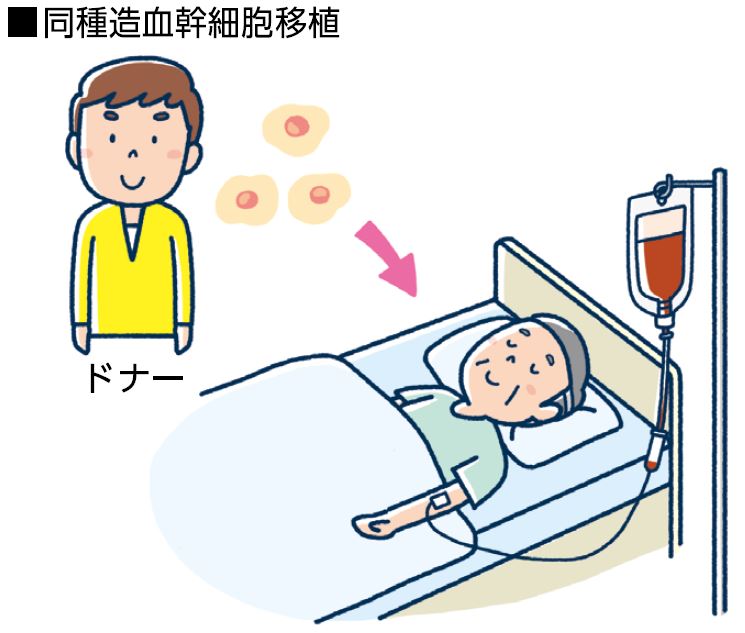
高リスクの患者さんについては、原則として55 歳以下で全身状態が良好ならば同種造血幹細胞移植が推奨されます。「同種」とは「同じ種類の生物」という意味で、今のところ骨髄異形成症候群の完治が望める唯一の治療法です。化学療法や全身への放射線照射などの移植前処置のあと、ドナーから採取した造血幹細胞を点滴で投与します。
ドナーは、HLA(ヒト白血球抗原)の型が適合する確率の高い血縁者から探し、見つからなければ骨髄バンクや、さい帯血バンクで探します。
近年では親子間など、HLAの一致が半分だけでも、移植が可能となりました。
60代以上の高齢者や持病のある患者さんは強力な移植前処置に耐えられないため、抗がん剤や放射線照射の量を抑えたミニ移植が検討されます。再発の問題は残るもののメリットは大きく、一部の医療機関では80代の人にも行われています。
ドナーから提供を受ける同種移植では、移植後の合併症や副作用が問題となります。ドナー由来のリンパ球が患者さんの正常臓器を異物とみなして攻撃する移植片対宿主病(GVHD)、免疫力低下に伴う感染症などは命にかかわりますが、新薬や移植技術の向上によって死亡率は低下してきています。
低リスクの患者さんでも、病状が進んで高リスクの範囲に入ってくれば移植が検討されます。輸血の効果が落ちて輸血回数が多くなり、仕事や生活に支障をきたすようになった場合も、やはり移植が選択肢になり得ます。
条件的に移植が難しい高リスクの患者さんには抗がん剤のアザシチジンが使われます(皮下注射または点滴)。2011年に認可されたもので、対症療法や化学療法よりも生存期間を延ばしたり、急性骨髄性白血病への移行を遅らせたりする効果があります。副作用が穏やかなのもメリットです。
感染対策はこまめに 早期発見には血液検査
骨髄異形成症候群は手ごわい病気です。自分1人で立ち向かおうとせず、家族のサポートを得ながら、前向きにこの病気と闘うことが重要です。日常生活では感染症対策についての医師の指導を守り、歯磨きやうがいなどの口腔ケア、手洗いをこまめに行い、発熱があればすぐに受診してください。インフルエンザや新型コロナウイルス感染症の流行期は人混みを避けたほうがよいでしょう。
運動にも注意が必要です。貧血になると体が酸欠状態になるため、それを補おうとして心臓に負担がかかり、心不全のリスクが上昇します。激しい運動は避け、医師と相談しながら無理のない有酸素運動を心がけましょう。
重篤な感染症などの合併症を回避するには早期発見、早期治療がカギです。高齢者で冒頭に紹介したような自覚症状があれば、「年のせい」などと軽視せず、血液検査を受けてみましょう。
ライター 平野 幸治